Lei de Proust (Lei das proporções constantes)
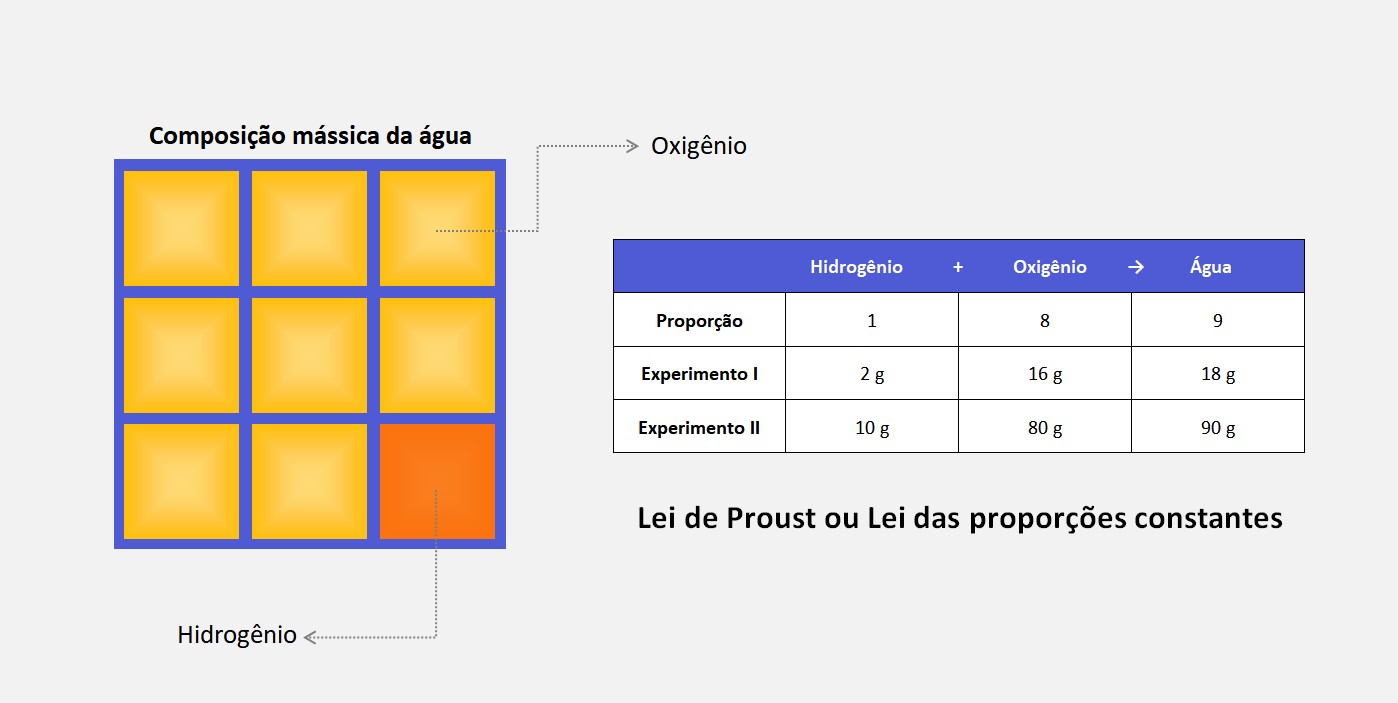
A Lei de Proust, também conhecida como Lei da Definitividade dos Compostos, é uma regra em química que afirma que um composto puro sempre terá a mesma composição, independentemente da origem ou do método de preparação.
Essa lei foi formulada pelo químico francês Joseph Louis Proust (1754-1826) no final do século XVIII. Proust realizou uma série de estudos para determinar a proporção em que os elementos se combinam para formar compostos. Ele descobriu que os elementos sempre se combinam em proporções fixas e definidas.
Essa lei é fundamental para o desenvolvimento da química e da ciência dos materiais, pois permite prever a composição dos compostos e relacionar as proporções em que os elementos se combinam.
No entanto, é importante ressaltar que a Lei de Proust não é absoluta e existem casos em que as proporções não são tão exatas.
Por exemplo, existem compostos conhecidos como isótopos, nos quais a proporção dos elementos pode variar ligeiramente devido à presença de diferentes isótopos dos elementos envolvidos.
Apesar disso, a Lei de Proust continua sendo uma regra fundamental na química e permite estabelecer os fundamentos da estequiometria, relacionando as quantidades de reagentes e produtos em uma reação química. É uma base essencial na compreensão da formação e transformação de substâncias químicas.