Ligações de hidrogênio
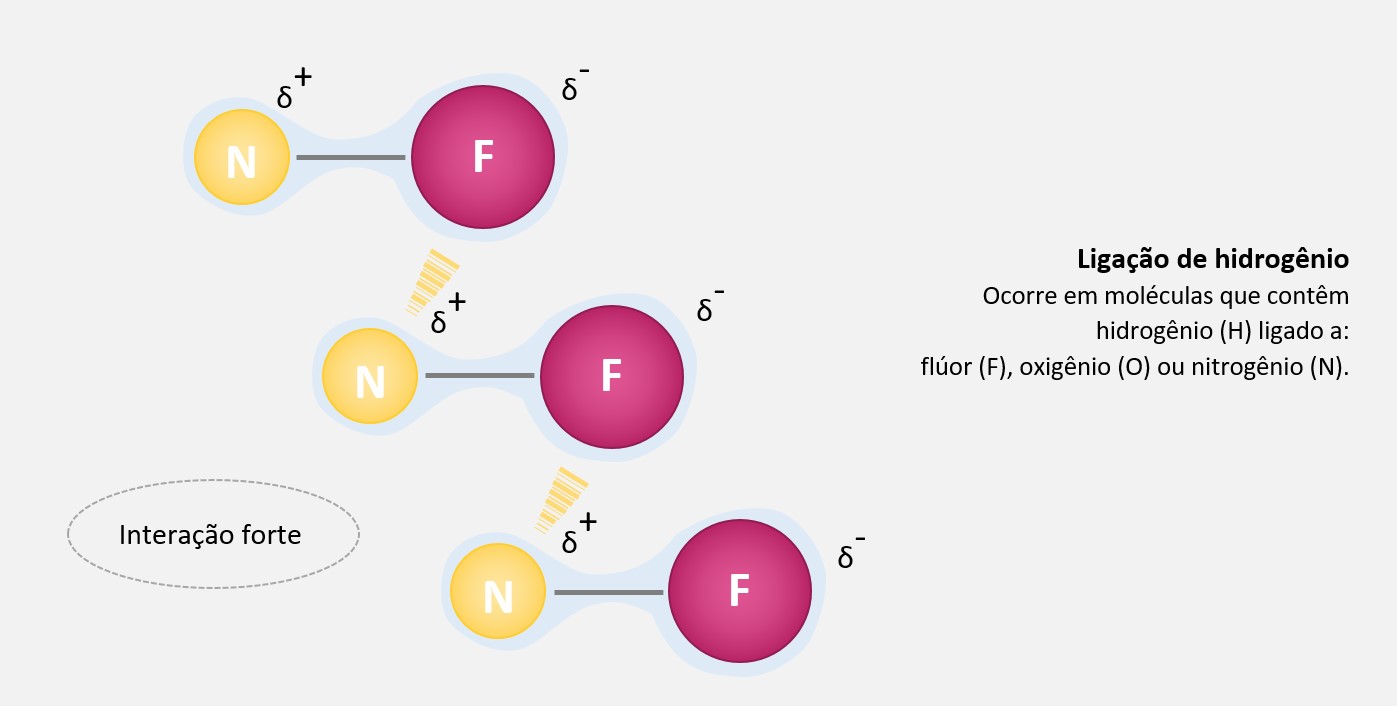
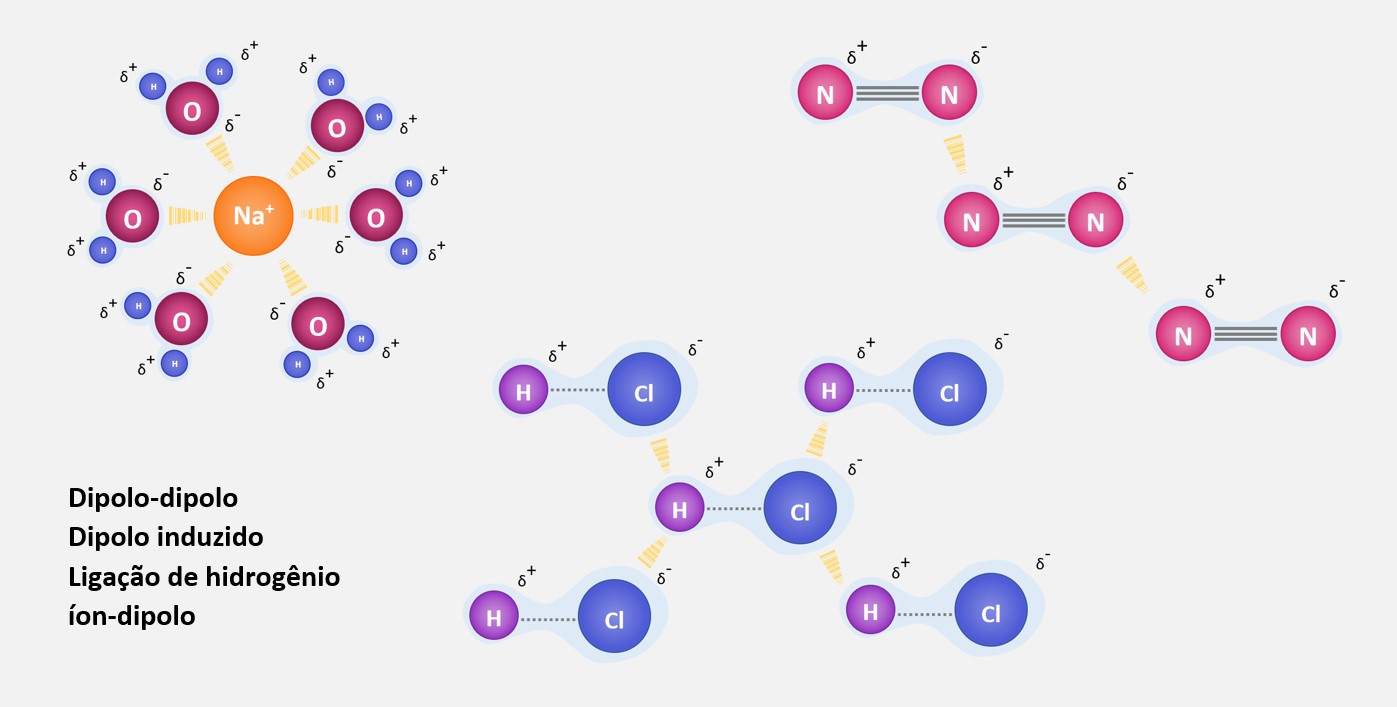
Ligações de hidrogênio, também conhecidas como pontes de hidrogênio, são tipos especiais de ligações intermoleculares que ocorrem entre uma molécula polar contendo um átomo de hidrogênio ligado a um átomo eletronegativo (como oxigênio, nitrogênio ou flúor) e outro átomo eletronegativo.
As ligações de hidrogênio são responsáveis pelo comportamento único e muitas vezes excepcional de várias substâncias, especialmente aquelas com hidrogênio ligado a oxigênio, nitrogênio ou flúor. Elas têm um papel fundamental em diversas propriedades, como pontos de ebulição e fusão elevados, solubilidade, viscosidade e a estrutura tridimensional de macromoléculas biológicas, como proteínas e DNA.
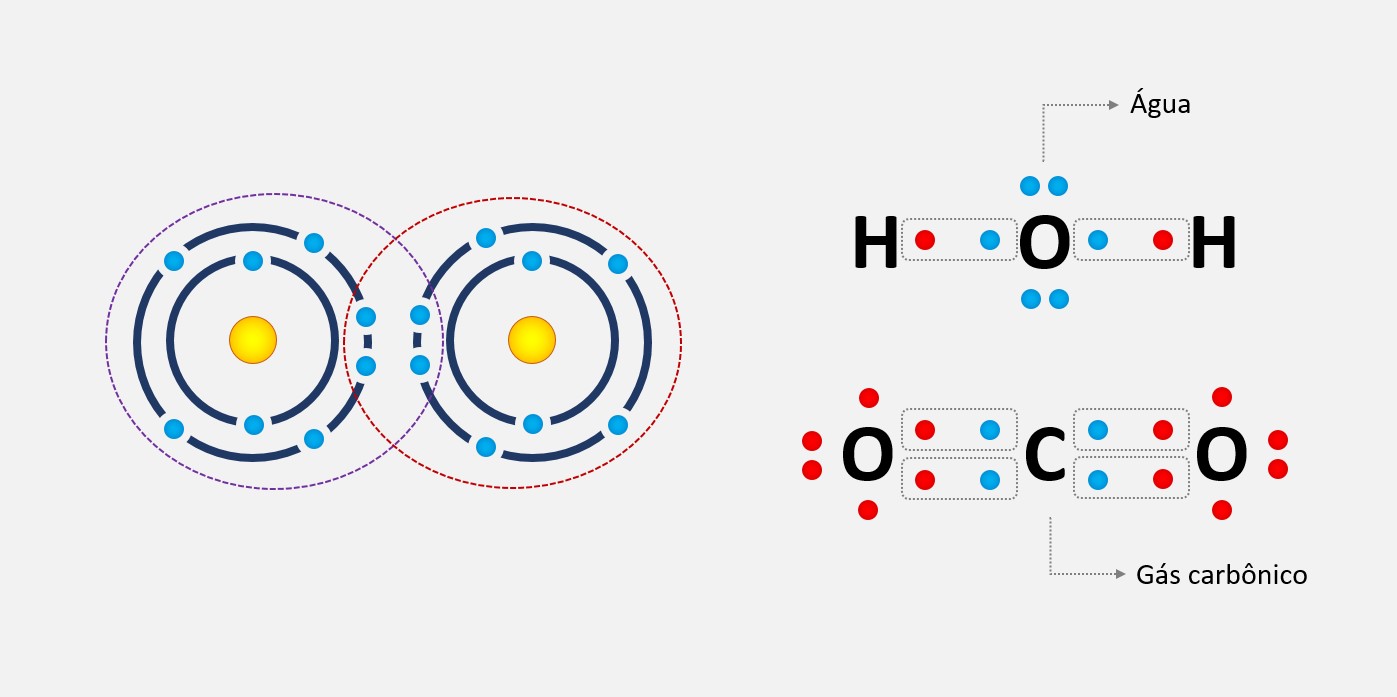
Um exemplo clássico de ligação de hidrogênio ocorre na molécula de água (H2O), em que o hidrogênio ligado ao oxigênio forma uma ponte de hidrogênio com o oxigênio de outra molécula. Essas ligações de hidrogênio conferem várias propriedades únicas à água, como sua alta tensão superficial, capacidade de se dissolver em muitas substâncias e comportamento anômalo de expansão térmica.