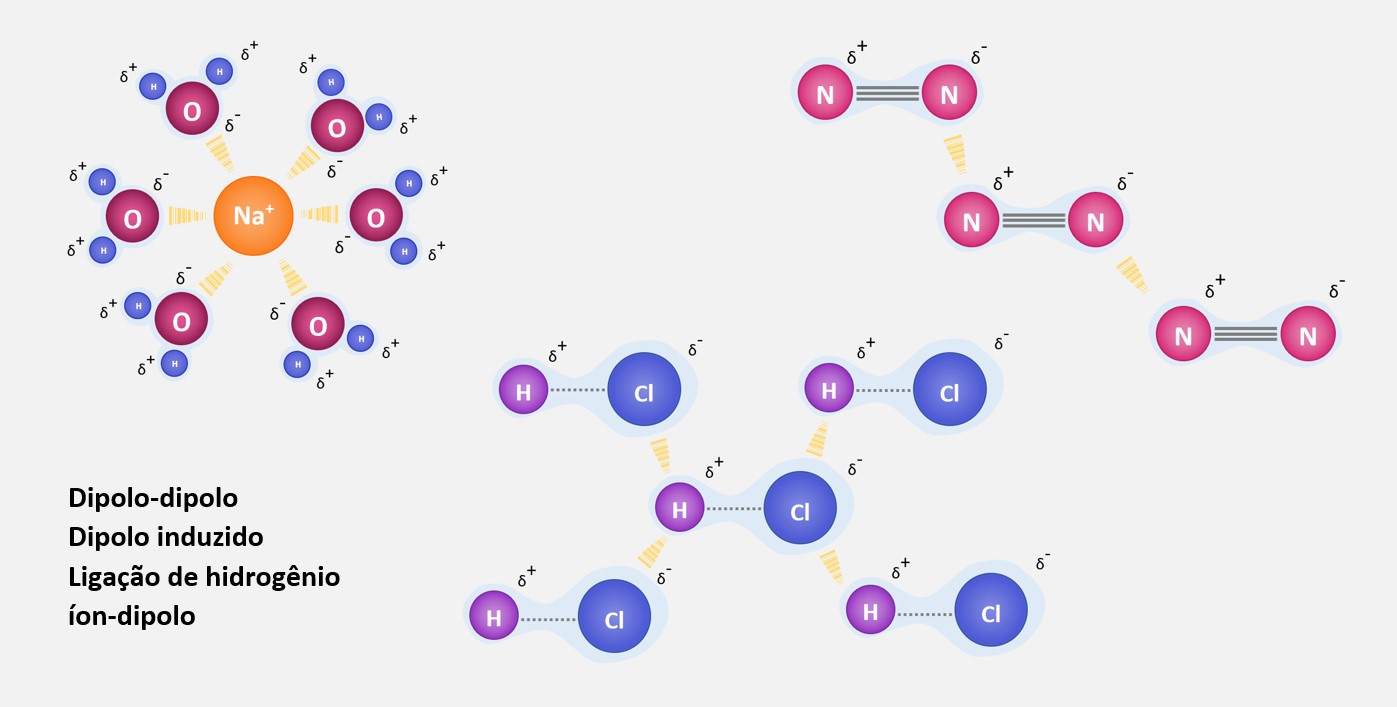
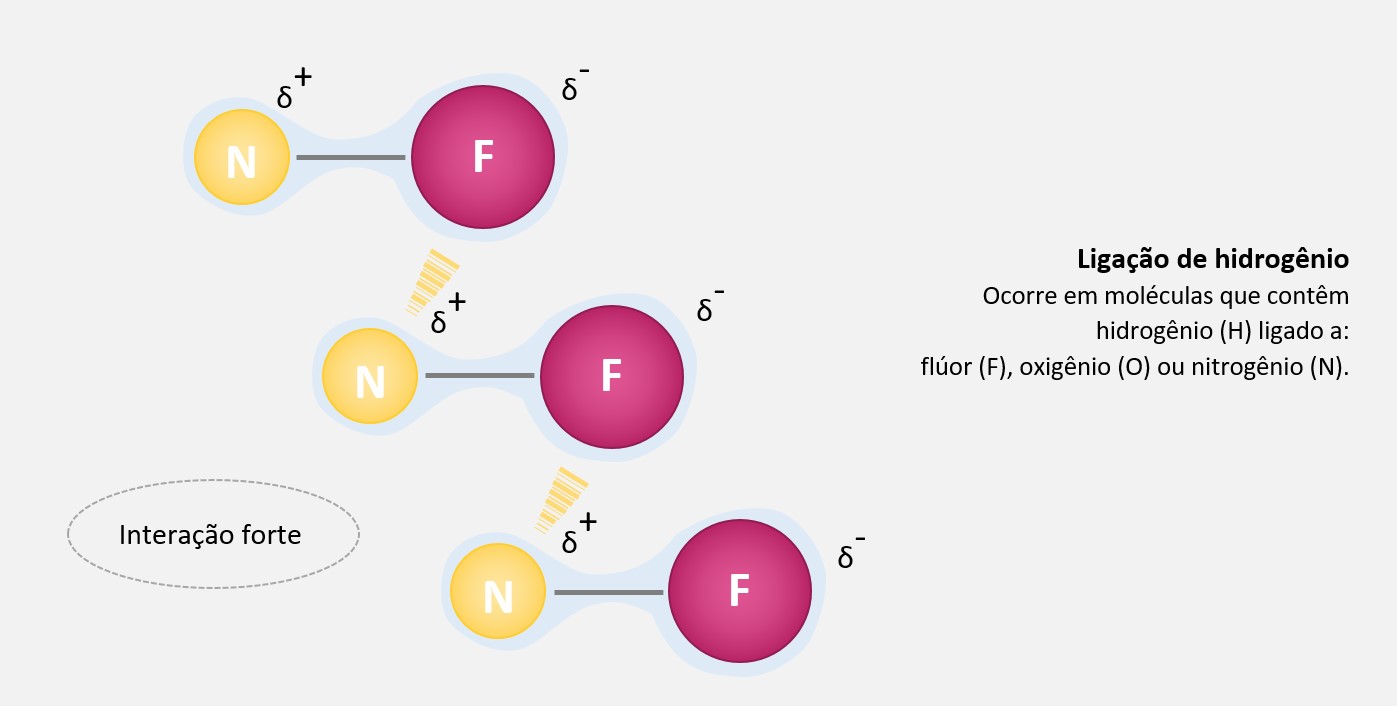
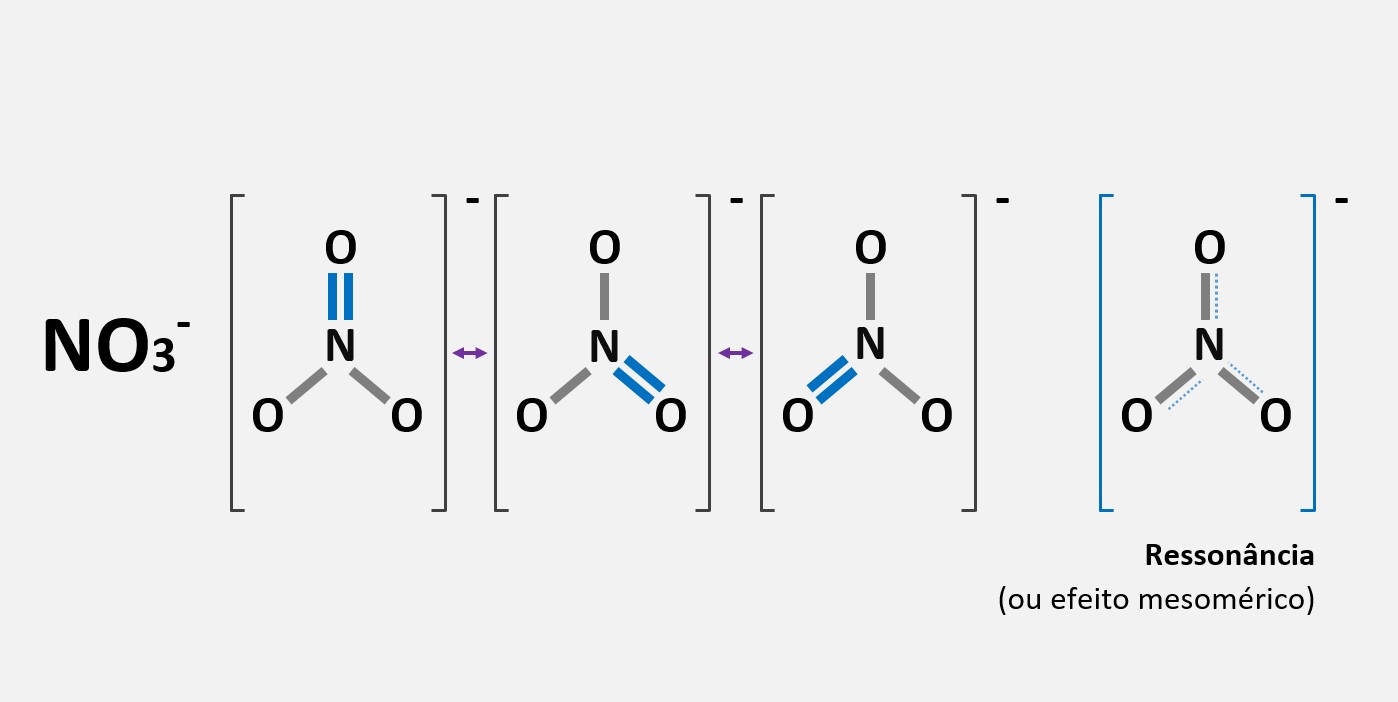
Ligação covalente
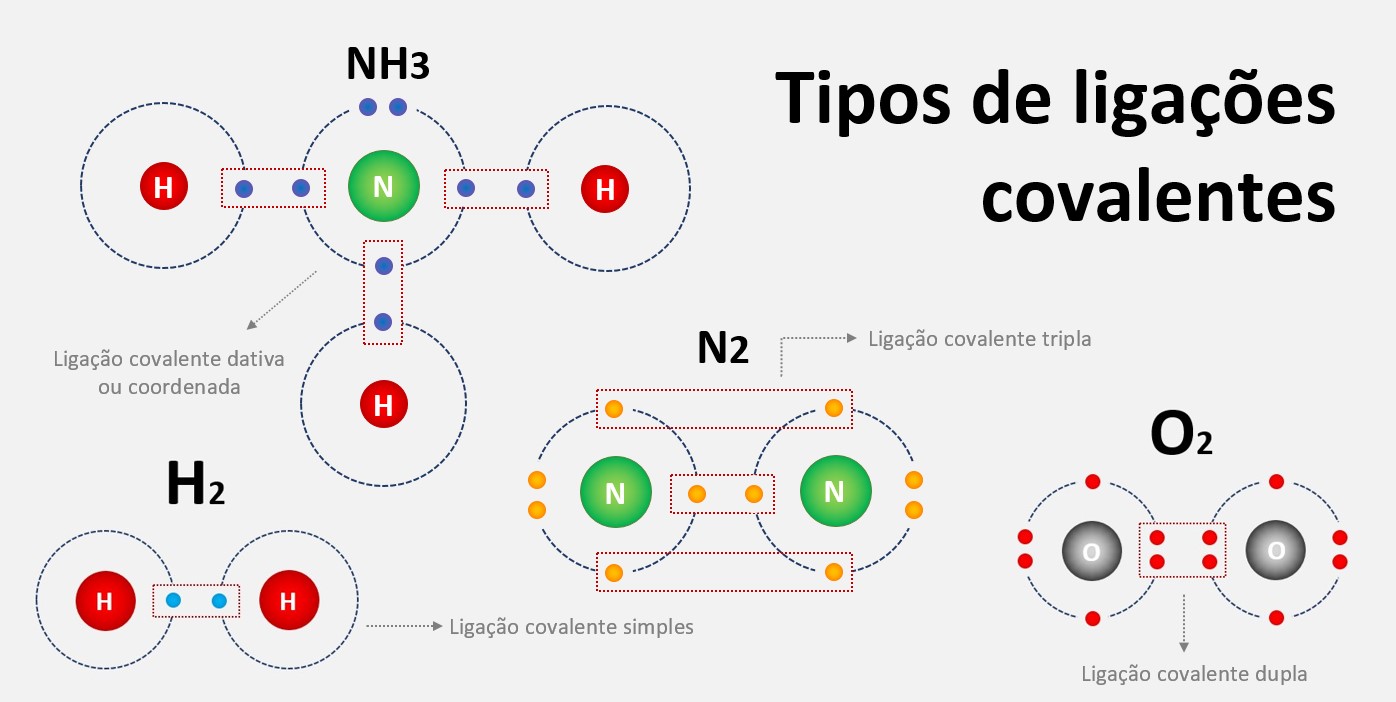
Existem quatro tipos de ligação covalente: simples, dupla, tripla e dativa.
1. Ligação covalente simples: É a ligação mais básica entre dois átomos. Nesse tipo de ligação, os átomos compartilham um único par de elétrons, formando uma ligação simples.
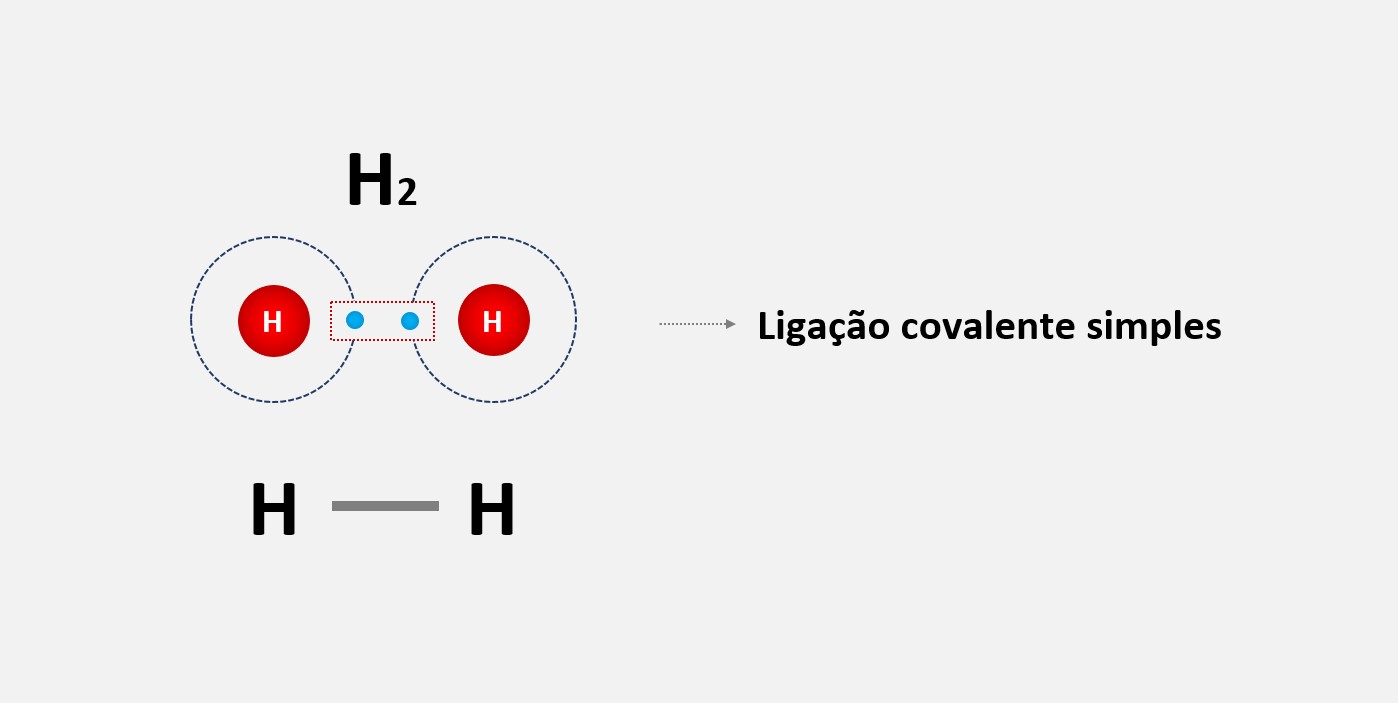
2. Ligação covalente dupla: Nesse tipo de ligação, os átomos compartilham dois pares de elétrons. É representada por uma linha dupla entre os átomos na estrutura de Lewis.
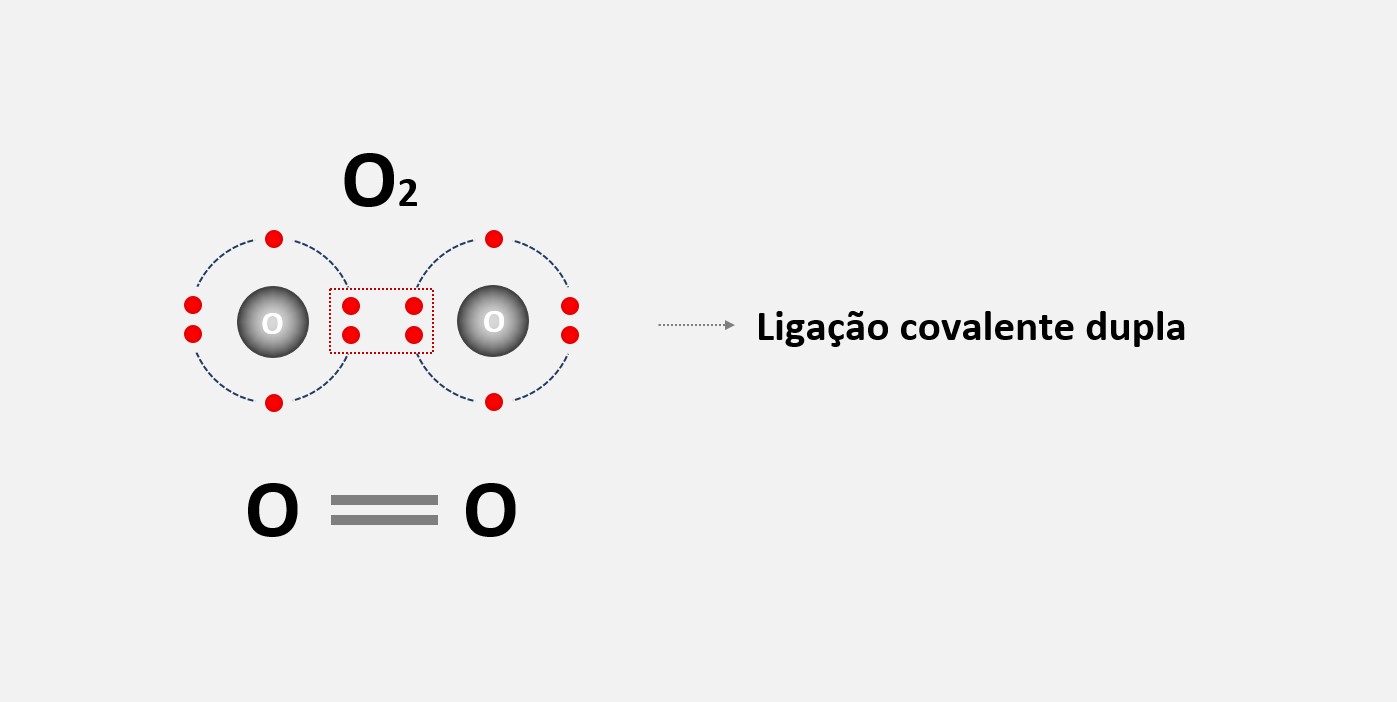
3. Ligação covalente tripla: Nesse tipo de ligação, os átomos compartilham três pares de elétrons. É representada por uma linha tripla entre os átomos na estrutura de Lewis.
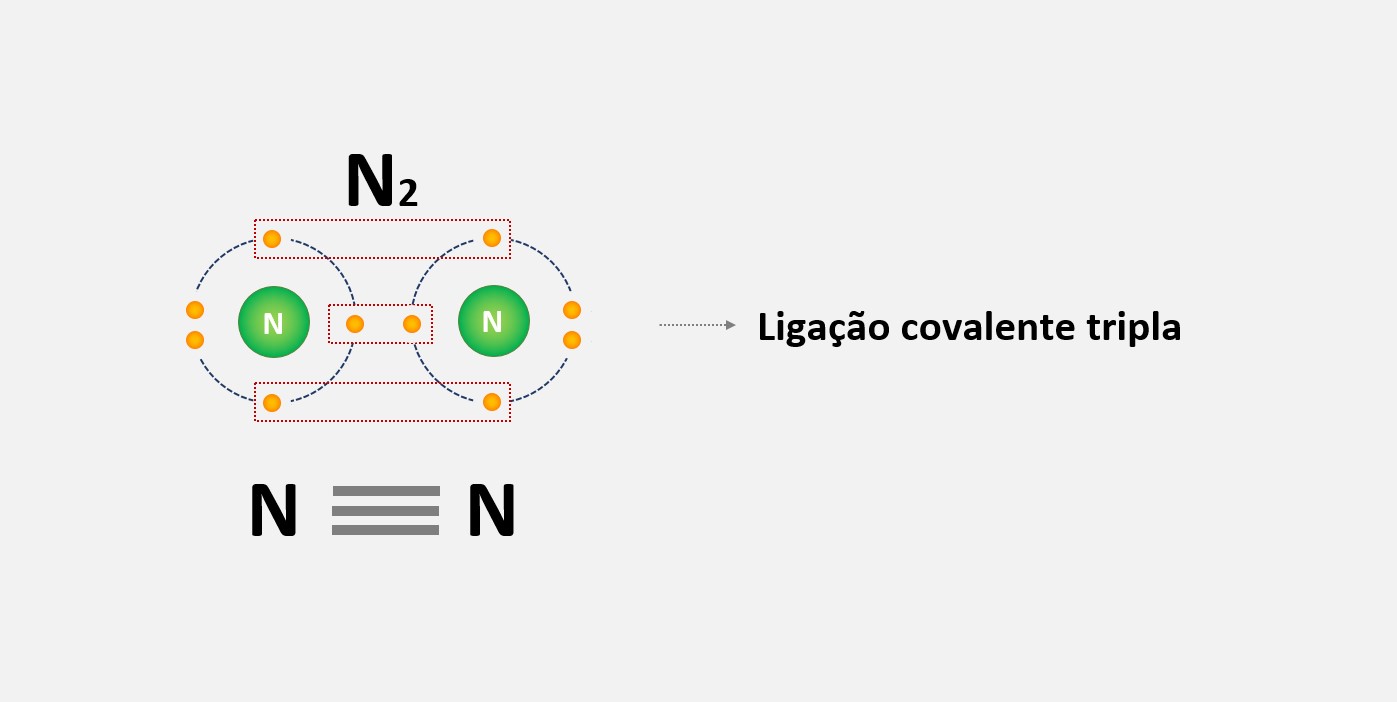
4. Ligação covalente dativa (ou coordenada): Nesse tipo de ligação, um dos átomos fornece ambos os elétrons para a ligação covalente. Essa ligação ocorre quando um átomo possui um par de elétrons não compartilhados e outro átomo precisa de um elétron adicional para completar sua camada de valência.
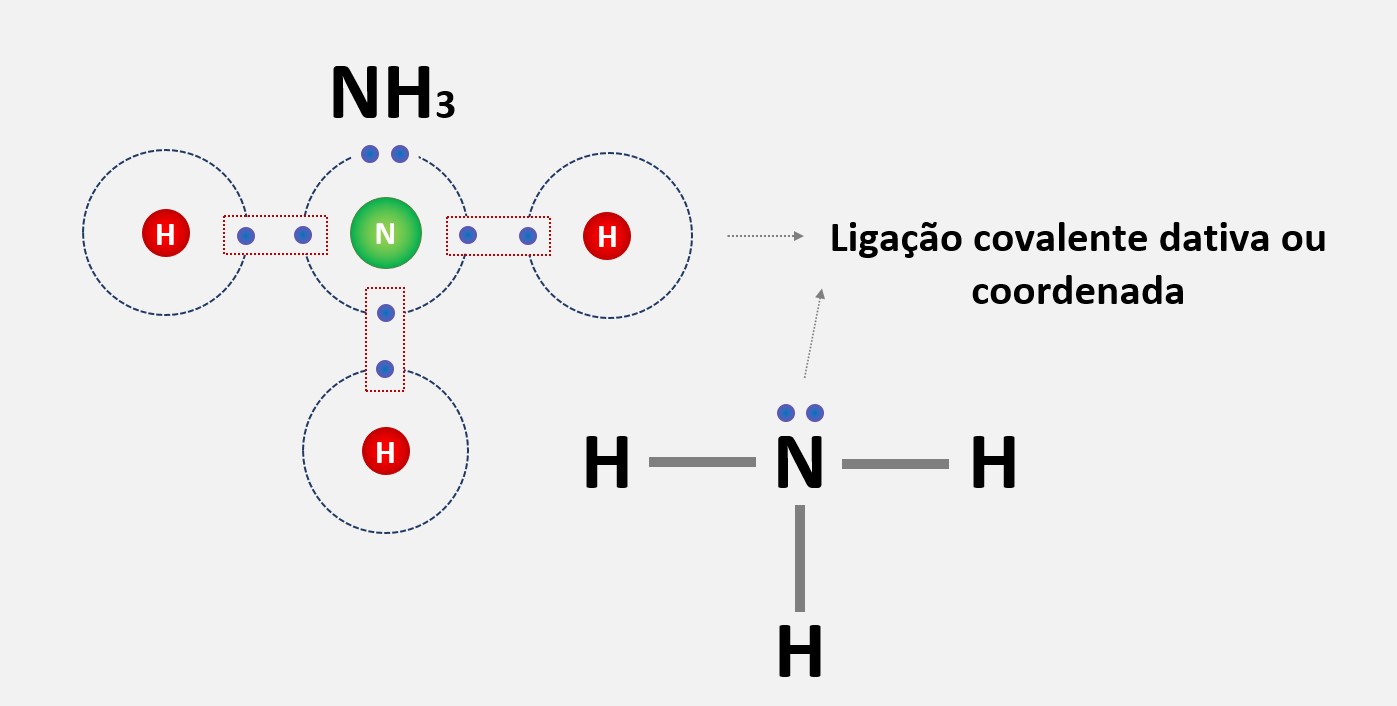
Esses quatro tipos de ligações covalentes podem ocorrer em diferentes combinações em moléculas complexas, dependendo dos átomos envolvidos e de como eles compartilham seus elétrons de valência.