A proteção catódica e a proteção anódica são utilizadas em diferentes situações, dependendo das características do material a ser protegido e do ambiente em que ele está exposto.
Esses revestimentos fornecem uma barreira física entre o metal e seu ambiente, impedindo que o oxigênio e a umidade entrem em contato com a superfície do metal. Além disso, eles também podem conter inibidores de corrosão, que são substâncias que diminuem a taxa de corrosão do metal.
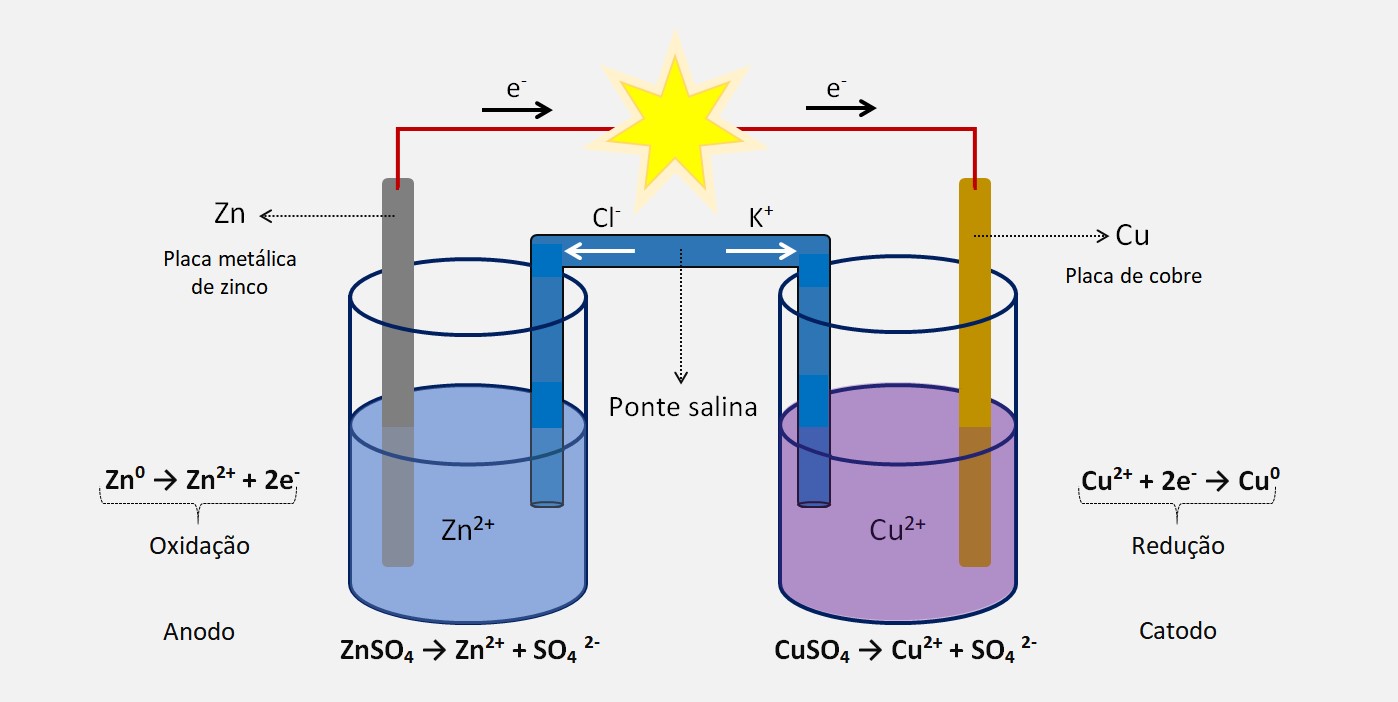
A proteção catódica é comumente usada em ambientes marinhos e em estruturas submersas, como tubulações, tanques de armazenamento e plataformas offshore. Nesses casos, são adicionados ânodos de sacrifício, como o zinco ou o magnésio, que são mais reativos do que o metal a ser protegido. Esses ânodos corroem preferencialmente, liberando elétrons que passam para o metal, impedindo assim a corrosão do mesmo. Esse processo é chamado de proteção catódica galvânica.
A proteção anódica, por sua vez, é usada em situações em que é necessário aplicar uma corrente elétrica para proteger o metal contra a corrosão. Isso normalmente é realizado pela aplicação de uma tinta condutora contendo óxidos metálicos, que atua como um ânodo. Quando uma corrente elétrica é aplicada, os íons metálicos da tinta são liberados e reagem com o oxigênio na atmosfera, formando uma película protetora sobre a superfície do metal. Essa técnica é comumente usada em indústrias, como a de petróleo e gás, onde há exposição a ambientes corrosivos.
Em resumo, a proteção catódica utiliza ânodos de sacrifício para proteger o metal, enquanto a proteção anódica utiliza uma corrente elétrica para criar uma camada protetora sobre o metal. Ambas as técnicas têm como objetivo prevenir a corrosão e prolongar a vida útil dos materiais metálicos.