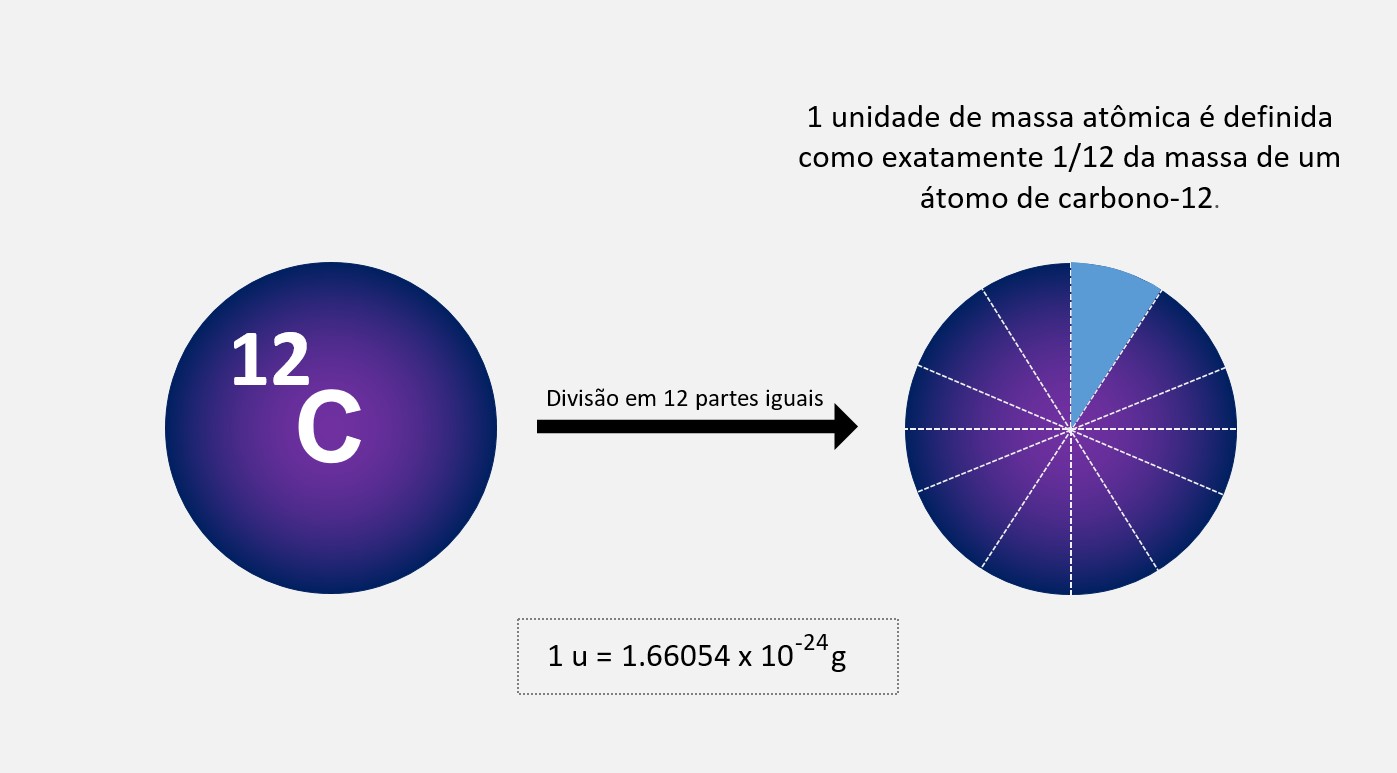
O que é abundância relativa?
A abundância relativa na química é uma medida que indica a proporção de um determinado elemento em uma amostra em relação aos demais elementos presentes na mesma amostra. É expressa geralmente em porcentagem. Por exemplo, se uma amostra contém 80% de carbono, 10% de oxigênio e 10% de hidrogênio, a abundância relativa do carbono é de 80%.
A abundância relativa também pode ser expressa como a quantidade relativa de um isótopo de um elemento em relação aos outros isótopos do mesmo elemento. Isso é especialmente relevante para elementos que possuem vários isótopos, como o carbono-12, carbono-13 e carbono-14. Nesse caso, a abundância relativa de um isótopo é a proporção de quantos átomos desse isótopo existem em relação ao total de átomos de carbono presentes na amostra.
Vamos considerar um exemplo de cálculo de abundância relativa para isótopos de carbono.
Suponha que uma amostra de carbono contenha três isótopos de carbono: carbono-12 (12C), carbono-13 (13C) e carbono-14 (14C).
1. Primeiro, determine as massas atômicas dos isótopos de carbono:
- 12C: massa atômica = 12 u
- 13C: massa atômica = 13,00335 u
- 14C: massa atômica = 14,00324 u
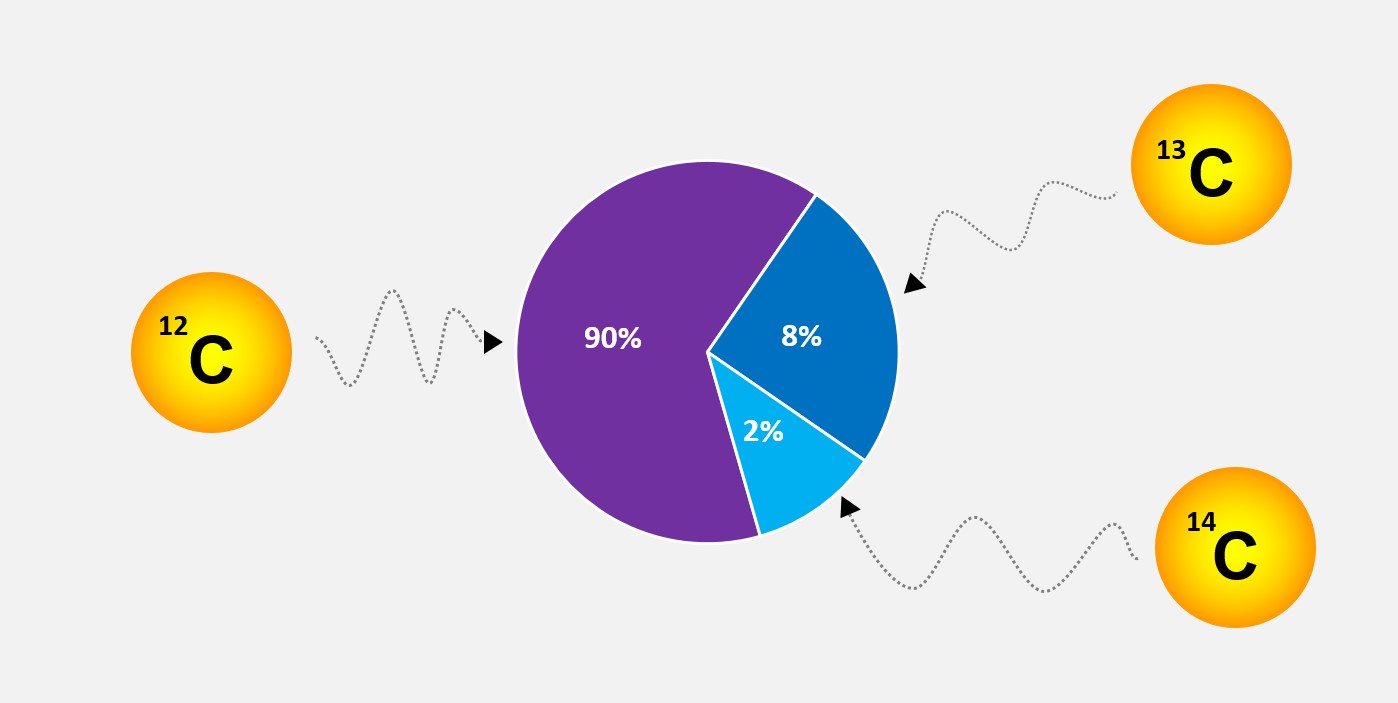
2. Em seguida, determine a abundância relativa de cada isótopo de carbono na amostra. Suponhamos que a amostra contenha 90 átomos de 12C, 8 átomos de 13C e 2 átomos de 14C.
- Para o isótopo de carbono-12 (12C):
Abundância relativa = [(número de átomos de 12C) / (total de átomos de carbono)] * 100
Abundância relativa = (90 / 100) * 100 = 90%
- Para o isótopo de carbono-13 (13C):
Abundância relativa = [(número de átomos de 13C) / (total de átomos de carbono)] * 100
Abundância relativa = (8 / 100) * 100 = 8%
- Para o isótopo de carbono-14 (14C):
Abundância relativa = [(número de átomos de 14C) / (total de átomos de carbono)] * 100
Abundância relativa = (2 / 100) * 100 = 2%
Portanto, a abundância relativa do isótopo de carbono-12 é de 90%, a do carbono-13 é de 8% e a do carbono-14 é de 2%.