Decaimento radioativo
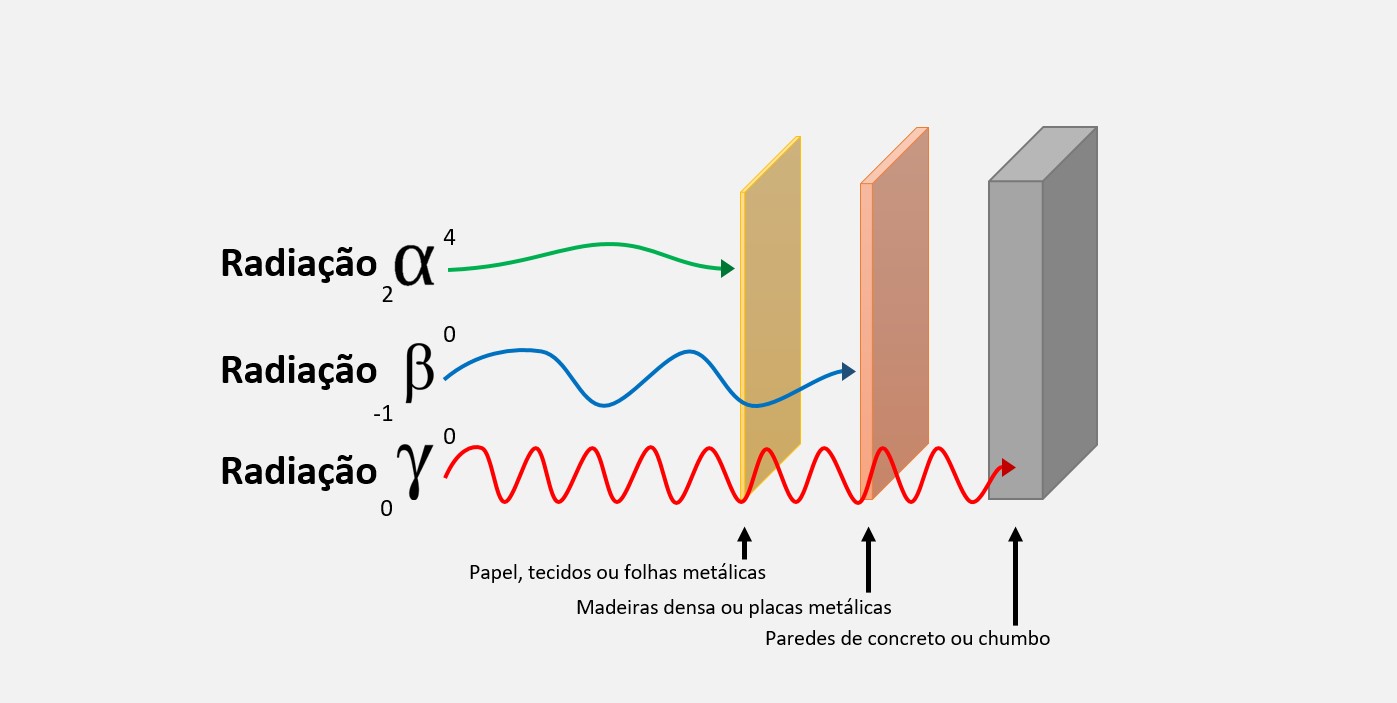
O decaimento radioativo é um processo pelo qual um núcleo atômico instável emite partículas ou radiação, transformando-se em um núcleo mais estável. Essa emissão acontece de forma aleatória e é caracterizada por uma meia-vida, que é o tempo necessário para que metade dos átomos de uma amostra radioativa se desintegre. Durante o decaimento radioativo, podem ser emitidas partículas alfa (dois prótons e dois nêutrons), partículas beta (elétrons ou pósitrons) ou radiação gama (radiação eletromagnética de alta energia). O decaimento radioativo é uma importante fonte natural de radiação e é utilizado em diversas aplicações, como em tratamentos médicos, na datação de fósseis e em usinas nucleares para gerar energia.
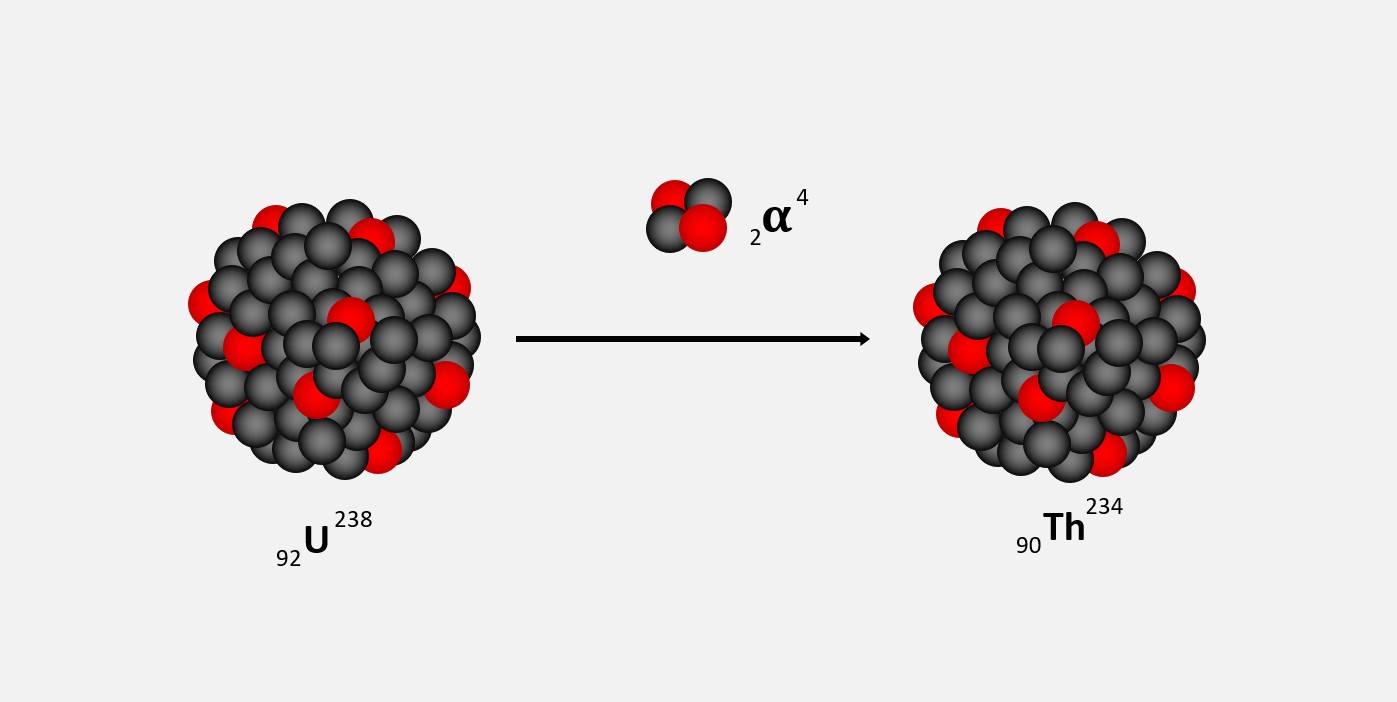
No decaimento alfa, um núcleo emite uma partícula alfa, que é composta por dois prótons e dois nêutrons. Isso resulta na redução de dois prótons e dois nêutrons no núcleo original. Esse processo faz com que o elemento se torne um novo elemento químico, pois a perda de partículas altera seu número atômico.
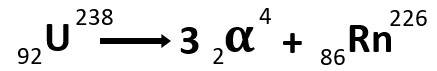
Quando um radioisótopo emite uma partícula alfa (α), consistindo de dois prótons e dois nêutrons, ele se transforma em outro elemento com um número atômico inferior em duas unidades e um número de massa inferior em quatro unidades. Essa é uma das formas de decaimento radioativo e é fundamental para entender as mudanças que ocorrem durante o processo de desintegração dos radioisótopos.
No decaimento beta, um nêutron é transformado em um próton ou um próton é transformado em um nêutron. Isso ocorre através da emissão de um elétron (decaimento beta negativo) ou um pósitron (decaimento beta positivo). Essa emissão de partículas causa uma alteração no número de prótons no núcleo e, portanto, pode resultar na formação de um novo elemento químico.
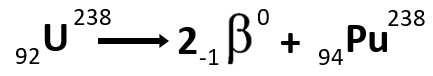
Está relacionada ao decaimento beta (β), também conhecido como emissão beta ou decaimento beta. Durante o decaimento beta, um nêutron no núcleo do radioisótopo se transforma em um próton, emitindo simultaneamente um elétron (β-) ou um pósitron (β+) e uma partícula menor chamada neutrino ou antineutrino.
O decaimento gama ocorre quando o núcleo emite radiação gama, que é uma forma de radiação eletromagnética de alta energia. Ao contrário do decaimento alfa e beta, o decaimento gama não altera a composição do núcleo, mas apenas libera energia excessiva. Os diferentes tipos de decaimento radioativo ocorrem de forma aleatória e são caracterizados por taxas de decaimento específicas, geralmente expressas como meia-vidas.
A meia-vida é o tempo necessário para que metade dos átomos de uma amostra radioativa se desintegre. Através do estudo do decaimento radioativo, é possível determinar a idade de fósseis, rochas e outros materiais, bem como utilizar fontes radioativas para aplicações médicas e industriais. Nesse processo de decaimento beta, o número atômico do elemento aumenta em uma unidade, enquanto o número de massa permanece inalterado. Portanto, o novo elemento produzido terá um número atômico maior, refletindo a mudança de um nêutron para um próton, mas o número de massa permanecerá o mesmo.