Modelo atômico de Rutherford-Bohr
O modelo atômico de Rutherford-Bohr foi uma proposta revolucionária para explicar a estrutura e o comportamento dos átomos, desenvolvida por Niels Bohr a partir das descobertas de Ernest Rutherford sobre a estrutura nuclear do átomo.
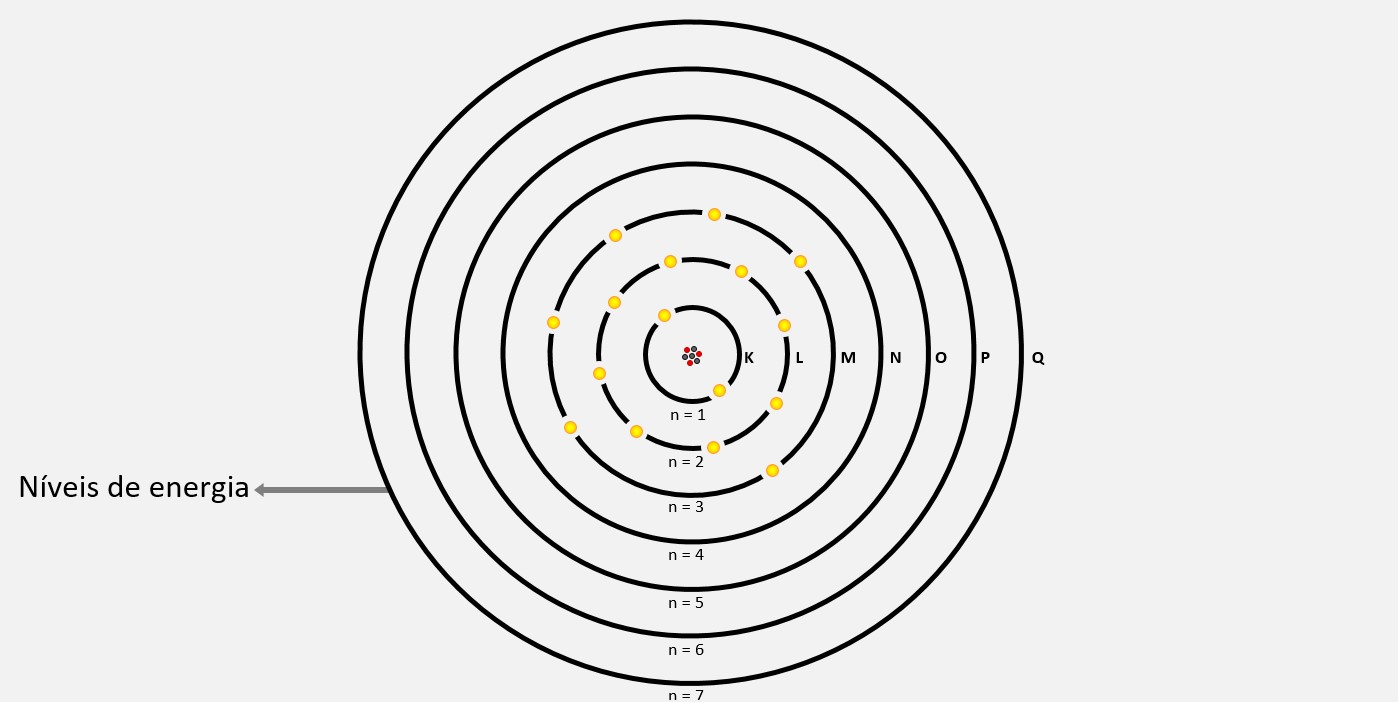
O modelo de Rutherford-Bohr introduziu a ideia de que os elétrons estão localizados em órbitas circulares ao redor do núcleo do átomo. Essas órbitas, que são chamadas de níveis de energia ou camadas eletrônicas, são quantizadas, ou seja, apresentam valores específicos de energia para os elétrons. Niels Bohr também relacionou os diferentes níveis de energia dos elétrons com as raias do espectro descontínuo dos gases.

Ele mostrou que, quando um elétron absorve um quantum de energia, ele salta para um nível de energia mais alto. E quando esse elétron retorna ao seu nível de origem, ele libera a energia absorvida na forma de uma onda eletromagnética, que pode ser observada como uma linha espectral característica no espectro descontínuo. Essa relação entre os níveis de energia dos elétrons e as raias espectrais permitiu explicar o fenômeno da emissão e absorção de luz por parte dos átomos.
Apesar de ter sido um modelo inovador e fundamentado experimentalmente, o modelo de Rutherford-Bohr foi posteriormente aprimorado pela teoria quântica-mecânica, que descreve o comportamento dos elétrons em termos de funções de onda e não mais de órbitas definidas.
No entanto, o modelo de Rutherford-Bohr foi uma etapa importante na compreensão da estrutura atômica e contribuiu significativamente para o desenvolvimento da física quântica.